Васкулиты представляют собой широкий спектр заболеваний имеющих разнообразную природу. Среди них первичные васкулиты имеют аутоиммунную этиологию, а другие процессы являются вторичными по отношению к опухолям, инфекциям и коагулопатиям.
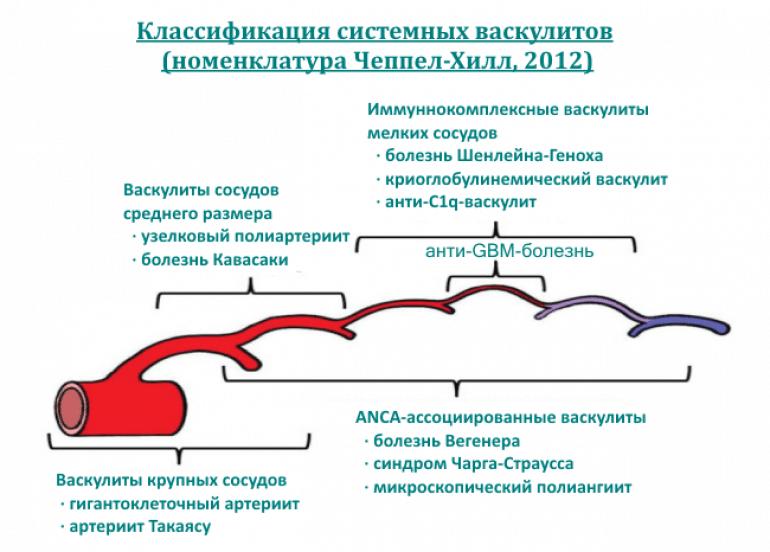
На основании классификации Chapel Hill 2012 года прервичные васкулиты делят по калибру пораженных сосудов и механизму иммунологического поражения. В основе патогенеза васкулитов крупных сосудов, к которым относятся аортоартериит Такаясу и височный артериит, лежит поражение сосудистой стенки, что обуславливает большую площадь вовлеченного эндотелия. Одной из причин воспаления сосудистой стенки является индукция антител к эндотелию (HUVEC). Синтез эндотелием провоспалительных цитокинов, прежде всего TNFa и IL-6, приводит к формированию выраженного острофазового ответа, выявление которого широко используется в диагностике васкулитов крупных сосудов. Так при аортоартерите Такаясу, височном артериите отмечаются чрезвычайно высокие уровни СРБ и значительно повышенные значения СОЭ.
Узелковый полиартериит является редкой формой системных васкулитов. Он может развиться в течении 1 года после перенесенного вирусного гепатита В. Обычно представляет собой самолимитирующее заболевание, которое рецидивирует крайне редко. Несмотря на то, что морфологически он проявляется гранулематозным воспалением, сходным с гранулемами при микроскопическом полиангиите, антинейтрофильные антитела (АНЦА) и другие специфические серологические маркеры при классическом узелковом полиартериите отсуствуют. Обычно его обострение сопровождается гипокомплементемией (С3 и С4), а также увеличением концентраций острофазовых белков (СРБ). В сыворотке крови пациентов обычно обнаруживают признаки текущей инфекции гепатита В в виде наличия антигенов HBsAg и HBeAg.
Болезнь Кавасаки поражает преимущественно детей до 10 лет. Клинические проявления включают лихорадку, лимфаденопатию, кожную сыпь, характерное покраснение языка и слизистой рта, а также васкулит, поражающий коронарные артерии. Большая часть случае болезни Кавасаки возникает спорадически, однако описаны вспышки этого заболевания, которые указывают на ее инфекционный характер. Антиэндотелиальные антитела отмечаются у 90% пациентов при этом заболевании и коррелируют с его активностью.
Гранулематозные васкулитах мелких сосудов имеют ряд общих черт, к которым относят поражение почек по типу олигоиммунного экстракапиллярного гломерулонефрита с полулуниями, полиневрит и легочный капиллярит. Основным методом серологической диагностики гранулематозных васкулитов является обнаружение антинейтрофильных цитоплазматических антител (АНЦА). Антитела этого семейства реагируют с белками азурофильных гранул нейтрофильных гранулоцитов. Значение АНЦА в патогенезе и диагностике гранулематозных васкулитов, позволило выделить отдельную группу, обобщенных под названием АНЦА-ассоциированные васкулиты. К ним относятся гранулематоз Вегенера, синдром Чарг-Штраусса, микроскопический полиартериит, быстропрогрессирующий гломерулонефрит с полулуниями.
По аналогии с выявлением антинуклеарного фактора (АНФ), при флюоресцентной микроскопии для обнаружения АНЦА можно отметить несколько типов свечения цитоплазмы клеток. С помощью метода иммунофлюоресценции отмечается два основных типа свечения АНЦА – цитоплазматический (цАНЦА) и перинуклеарный (пАНЦА), которые зависят от клеточных мишеней нейтрофильных антитител, поэтому имеет важное значение в постановке диагноза. Каждому из типов свечения соответствуют свои антигенные мишени. Для описания типов свечения обычно используются сокращения – цАНЦА и пАНЦА. Кроме того, могут выявляться нетипичные варианты антинейтрофильных антител. Целесообразно выявлять АНЦА совместно с АНФ, так как последние могут маскировать АНЦА.
При цитоплазматическом типе свечения (цАНЦА) основным антигеном является протеиназа 3 (ПР-3), реже причиной становятся антитела к другим ферментам гранул, прежде всего белку BPI. При выявлении перинуклеарного типа иммунофлюоресценции (пАНЦА), несколько чаще выявляются антитела против миелопероксидазой (МПО) – основного микробицидного фермента азурофильных гранул, генерирующим кислородные радикалы. Реже выявляются антитела к другим ферментам нейтрофильных гранул, таких как лактоферрин, эластаза и каптепсин G. Кроме того, при исследовании антинейтрофильных антител нередко выявляются высокие титры антинуклеарного фактора, что требует уточнения серологического спектра с помощью дополнительных тестов. Для повышения чувствительности серологического обследования пациентов с системными васкулитам действующие международные рекомендации требуют одновременного использования иммунофлюоресцентного теста, а также выявления антител к протеиназе-3 и антител к миелопероксидазе (Антинейтрофильные антитела (АНЦА, аМПО и аПР3).
К известным антигенным мишеням АНЦА относят протеиназу-3, лизоцим, миелопероксидазу, лактоферрин, эластазу, белок BPI и катепсин G. Разработанная ИФА панель антигенов позволяет в одном тесте выявить антитела к 7 антигенам и полуколичественно исследовать содержание каждого из них (Антитела к антигенам цитоплазмы нейтрофилов).
К группе заболеваний АНЦА-ассоциированых васкулитов иногда относят синдром Гудпасчера, так как АНЦА могут отмечаться у 10-15% пациентов с этим заболеванием, совместно с антителами к базальной мембране клубочка (БМК), выявление которых являются основным лабораторным методом его диагностики. Хотя синдром Гудпасчера не является системным васкулитом, он проявляется геморраггическим альвеолитом и быстропрогрессирующим гломерулонефритом, который сложно отличить от АНЦА-ассоциированного поражения почек. В связи с этим, выявление АНЦА и антитела к базальной мембране почек обычно используется совместно.
Иммунокомплексные васкулиты обусловлены образованием иммунных комплексов между аутоантителами и их антигенами в крови и сосудистой стенке. Иммунные комплексы, которые можно обнаружить в сыворотке крови называют циркулирующими иммунными комплексами (ЦИК). Предполагается, что снижение растворимости ЦИК приводит к их отложению в сосудистой стенке и развитию воспаления. Снижение растворимости при замедлении скорости кровотока и температуры приводит к тому, что иммунными комплексами поражаются преимущественно капилляры, прежде всего капилляры кожи. Криоглобулинемический васулит сопровождается появлением в крови криоглобулинов – резновидности ЦИК, которые преципитирую при температуре ниже 35-30 градусов Цельсия. К сожалению тесты, направленные на прямое определение ЦИК очень не специфичны и не рекомендуются для практического использования и постановки диагноза.
Другим механизмом поражения кожи являются антитела к С1q фактору комплемента, которые стабилизируют С3-конвертазу и приводят к активации комплемента в стенках мелких сосудах. Выявление повышенного содержания аутоантител к C1q у больного с кожным васкулитом указывает на диагноз гипокомплементемического васкулита. При системной красной волчанке обнаружение антител к C1q определяет риск гломерулонефрита. Увеличение содержания в динамике может отмечаться перед обострением волчаночного нефрита.
Отдельно выделяют методы позволяющие обнаружить отложения иммунных комплексов и комплемента непосредственно в пораженной ткани. Обнаружение отложений иммунных комплексов в ткани с помощью иммунофлюоресцентного исследования биопсии кожи позволяет объективизировать иммуннокомплексный процесс и обладает большей достоверностью, по сравнению с методами выявления ЦИК.
До недавнего времени отсутствие других диагностических подходов, кроме клинических и морфологических, в значительной мере затрудняло их выявление. Это нередко приводило к диагностическим ошибкам в связи с полиморфной клинической картиной и сходством симптоматики с системными заболеваниями соединительной ткани и другими неревматическими заболеваниями. Проведение иммунологического обследования на раннем этапе позволяет сократить время постановки окончательного диагноза и избавить от анализа зачастую неоднозначных клинических данных.
|
Диагностические тесты при васкулитах сосудов различного калибра |
|
|
Крупных сосудов (воспалительные) |
Антитела к эндотелию (HUVEC) Антинуклеарный фактор НEP-2 |
|
Средних сосудов (гранулематозные) |
Антинейтрофильные антитела (АНЦА) Антитела к миелопирокседазе Антитела к протеиназе-3 Антитела к базальной мембране клубочка |
|
Мелких сосудов (иммунокомплексные) |
Криоглобулины с активность РФ Антитела к фактору комплемента С1q Иммунофиксация парапротеинемий Биопсия кожи с иммунофлюоресцентным исследованием |
|
Другие методы: исследование факторов комплемента C3, C4, CH-50, серология вирусных инфекций (вирус гепатита С и гепатита В), иммуноглобулины сыворотки IgG, IgM, IgA |
|
С более подробным описанием лабораторных тестов, использующихся для диагностики васкулитов, можно ознакомиться здесь.
Болезнь Бехчета (ББ) представляет собой системное аутоиммунное воспалительное заболевание, характеризующееся васкулитом и тромбозом артерий и вен всех размеров. Было показано, что развитие ББ ассоциировано с наличием у пациентов аллели B51 гена HLA (HLA-B51). Заболевание встречается во всех странах, но особенно распространено в регионах, располагавшихся в прошлом в области пролегания Шелкового пути. Заболеваемость ББ, таким образом, сильно варьирует и составляет 0,5 – 370 случаев на 100000 человек в год.
Для болезни Бехчета характерны системные проявления, которые могут затрагивать все системы и органы, что значительно усложняет постановку диагноза:
• Поражение кожных покровов и слизистых оболочек. Болезненные герпетиформные или афтозные язвы на слизистых и коже ротовой полости и половых органов являются характерным признаком ББ. Кроме этого, часто наблюдается узелковая эритема, а также изъязвления вне гениталий.
• Офтальмологические нарушения. Для ББ характерны следующие состояния, поражающие глаз: передний и задний увеит, гипопион, глаукома, синехии, васкулит и геморрагии сетчатки.
• Неврологические нарушения. При ББ наблюдаются нарушения когнитивных функций и памяти, дизингибиция, судороги, ишемическое поражение головного мозга, менингоэнцефалит, лимфоцитарная инфильтрация оболочек мозга, демиелинизация.
• Васкулопатия. Васкулит артерий всех размеров, аневризмы легочных артерий, аневризмы крупных артерий, тромбозы артерий и вен, поверхностный тромбофлебит, синдром Бадда-Киари.
• Поражение суставов. Ассиметричная артропатия и артрит без деформаций встречается у 60% пациентов. Чаще всего наблюдается поражение коленных суставов, суставов пясти и запястья, голеностопных суставов и локтевых суставов.
• Поражение желудочно-кишечного тракта (ЖКТ). При ББ чаще всего поражается пищевод и илиоцекальная часть кишечника. Обнаруживаются изъязвления, которые гистологически схожи с паттерном поражения при воспалительных заболеваниях кишечника.
• Почки. При ББ может наблюдаться гломерулонефрит с развитием нефритического синдрома.
• Другие проявления. Перикардит, миокардит, эндокардит, плеврит также могут наблюдаться при ББ.
Отсутствие аллели HLA-B51 значительно снижает риск развития болезни Бехчета у пациента, но не исключает его полностью. У пациентов с критериально подтверждённой болезнью Бехчета, но без аллели HLA-B51 реже наблюдаются язвы на слизистых, увеит и поражение кожи.
HLA-B51 имеет 200 подтипов, из которых HLA-B51:01 является наиболее распространенным. Тестом выявляются большинство подтипов, но есть исключения (например подтип HLA-B51:05). Было показано, что у 70% пациентов с ББ обнаруживается ген HLA-B51, и носительство данного гена значительно увеличивает риск развития заболевания. Было показано, что у пациентов с ББ положительных на HLA-B51 чаще наблюдаются язвы на слизистых, увеит и поражение кожи.