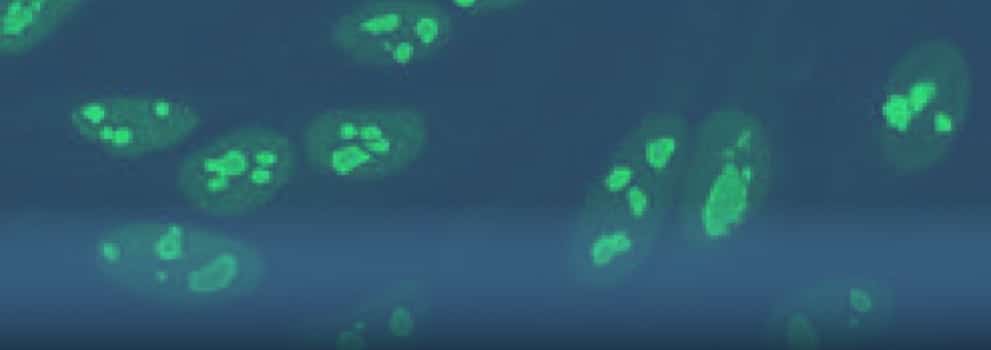
Лабораторное исследование антинуклеарных антител.
Основной задачей лабораторного тестирования антинуклеарных антител (АНА) является определение всех разновидностей аутоантител, присутствующих в конкретном образце. Методы выявления АНА делят на скрининговые, которые детектируют присутствие или отсутствие АНА в образце, и подтверждающие, результатом которых является определение спектра специфичностей АНА. Скрининговые тесты для выявления АНА используют для ранней диагностики системных заболеваний соединительной ткани (СЗСТ), а также исключения диагноза СЗСТ в случае неопределенной клинической картины. В тестировании АНА особое значение имеет метод непрямой иммунофлюоресценции (антинуклеарный фактор), в котором антитела выявляются за счет связывания с антигенами внутри клеток или тканевого субстрата. Термин антинуклеарный фактор (АНФ) обобщает тесты для скринингового выявления АНА, основанные на методе непрямой иммунофлюоресценции. Антитела выявляются за счет их связывания с клетками клеточных линий (реже криосрезами тканей лабораторных животных). Исторически использовался ряд клеточных и тканевых субстратов для выявления АНФ, но в настоящее время, повсеместно используется клеточная линия эпителиоидных клеток аденокарциномы гортани человека НЕр2. Распределение антигенов внутри клетки определяет тип свечения ядра, который позволяет судить о спектре АНА, присутствующих в данной сыворотке. Не всегда при наличии даже высоких тиров АНФ можно установить антигенную специфичность АНА, поскольку многие антигены, выявляющиеся с помощью АНФ, относят к конформационным (т. е. нестойким) и до сих пор плохо охарактеризованы. На отечественном рынке реактивы для определения АНФ представлены рядом производителей, например Euroimmun AG (Германия), Immco (США), BioSystems (Испания), Medipan AG (Германия). Преимуществами продукции Euroimmun AG является использование клеточной линии Нер-2000, обладающей повышенным числом клеточных делений, а также возможность совместного иммунофлюоресцентного исследования в одном реакционном поле других субстратов, например печени приматов, что повышает выявляемость ряда специфичностей АНА. Кроме АНФ применяют скрининговые тесты, основанные на выявлении антител к смеси антигенов ядер, очищенных из клеток или полученных методами генной инженерии. До недавнего времени для описания спектра АНА в иммунологических лабораториях, использовался экстрагируемый ядерный антиген (ЭНА), представляющий водно-солевые экстракты ядер клеток. В состав ЭНА входят растворимые клеточные антигены, прежде всего рибонуклеопротеины, однако водонерастворимые антигены, например нуклеиновые кислоты, в составе ЭНА отсутствуют. В настоящее время, под названием антитела к ЭНА обычно подразумевают выявление антител к смеси рекомбинантных антигенов. Проведение дифференциальной диагностики в рамках СЗСТ требует определения отдельных специфичностей АНА. Для определения специфичностей АНА существует широкий спектр методов и принципов детекции аутоантител, причем этот перечень постоянно расширяется. Современные молекулярно-биологические методы позволяют получать большой набор очищенных аутоантигенов, что значительно облегчает разработку новых тестов. Ведущими мировыми производителями создаются автоматизированные полузакрытые и закрытые системы, основанные на различных принципах: методе ИФА, дот- и лайн-блоты, хемилюминесцентный метод, мультиплексный анализ на микрочастицах и др. (таблица 1).

Несмотря на совершенствование методов, лайн-блоты представляют собой сравнительно дешевую, но достаточную надежную альтернативу автоматизированным технологиям для лабораторий с небольшим потоком исследований. Большинство лайнблотов, представленных на отечественном рынке, позволяет выявлять от 9 до 20 различных аутоантител в одном тесте, что обеспечивает значительное преимущество перед другими технологиями по спектру определяемых показателей. Так для диагностики СЗСТ фирма Euroimmun AG (Германия), выпускает линейку иммуноблотов с возможностью выявления до 30 специфичностей АНА. Разработаны продукты как для дифференциальной диагностики всех СЗСТ, так и для дифференциальной диагностики в рамках системной красной волчанки (СКВ), склеродермии, полимиозита. Возможность денситометрии с помощью оптических систем ряда офисных сканеров обеспечивает возможность количественной и полуколичественной оценки результатов блотов, а также возможность архивации результатов исследований (программа EUROLineScan). Внедрение современных автоматизированных систем ставит вопрос о целесообразности сохранения АНФ в качестве основного метода диагностики АНА. Несмотря на большую аналитическую чувствительность иммунометрических методов по сравнению с непрямой иммунофлюоресценцией на тканевых субстратах, спектр выявляемых АНА с помощью таких методов ограничен. Ограниченный спектр выявляемых специфичностей АНА обуславливает меньшую диагностическую чувствительность иммунометрических мультиплексных тестов по сравнению с АНФ, т. е. при использовании таких методов высока вероятность ложно-отрицательного результата. Наши данные свидетельствуют о том, что при определении АНА, например с помощью лайнблота, теряется до 9% и 50% положительных результатов в высоких и средних титрах АНФ соответственно. Именно поэтому АНФ до сих пор является «золотым стандартом», использование которого обеспечивает наиболее корректные результаты при выявлении АНА.
Международные рекомендации 2014 года
Для исследования АНА в клинической лаборатории может быть использовано множество диагностических тестов, основанных на разных принципах. Единой номенклатуры этих тестов не существует, что приводит к определенным затруднениям при назначении и интерпретации обследования. Фирмы-производители реактивов и оборудования для клинической лабораторной диагностики могут предлагать различные методические подходы к скринингу АНА и определения основных специфичностей. При этом выявление АНА постепенно покидает стены высокоспециализированных иммунологических лабораторий, что может привести к снижению качества обследования в угоду большей технологичности и пропускной способности метода. Несмотря на важность выявления АНА, до недавнего времени не существовало международных рекомендаций, регламентирующих методы выявления АНА в клинической лабораторной диагностике. Международные рекомендации по выявлению АНА были опубликованы недавно. В их подготовке принимали участие две группы экспертов. Наиболее многочисленной действующей группой, которая включала экспертов из 15 Европейских стран, является «Европейская аутоиммунная инициатива по стандартизации» (European Autoimmunity Standardization Initiative — EASI). Под ее эгидой проводится значительное количество конференций и круглых столов по вопросам диагностики аутоиммунных заболеваний (www.easinetwork.com). Другой международной организацией является совместный комитет Международного союза иммунологических обществ (IUIS), Всемирной организации здравоохранения (ВОЗ/WHO), Фонда артрита (AR), Центра по контролю и предотвращению заболеваемости США (CDC) и Американского колледжа ревматологов (ACR). «Совместный комитет по стандартизации аутоантител при ревматических и близких заболеваниях» (IUIS/WHO/ AR/CDC) более тридцати лет разрабатывает и внедряет стандарты и референтные сыворотки для выявления аутоантител (www.autoab.org). Опубликованные международные методические рекомендации охватывают основные методические вопросы организации лабораторного выявления АНА (таблица 2).
Данные методические рекомендации разделены на 3 блока вопросов. Первые 13 рекомендаций касаются методов выявления АНФ и регламентируют его использование, следующие 5 затрагивают выявление антител к двуспиральной ДНК и, наконец, последние пять пунктов определяют подходы к выявлению антител к ЭНА и специфичностей АНА. Рекомендации подчеркивают важность АНФ как референтного теста для скринингового выявления АНА, а также указывают на важность определения типа свечения ядра клетки.
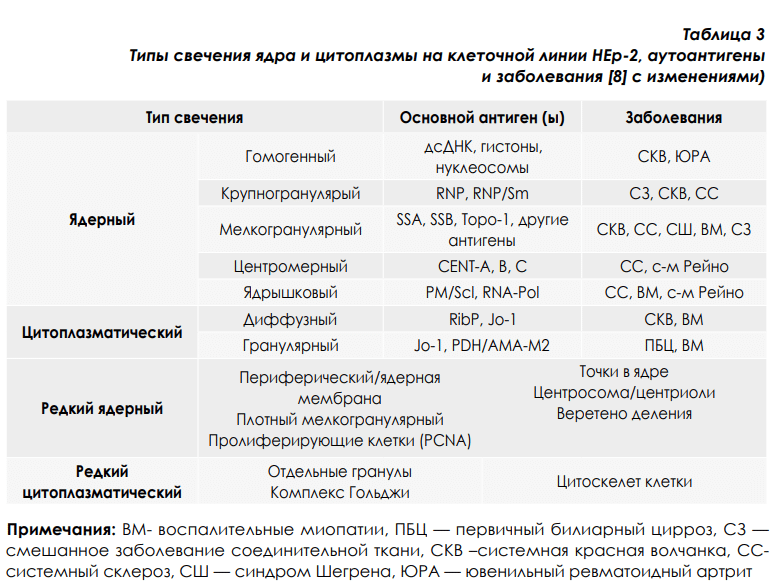
Тип свечения клетки позволяет планировать дальнейшее тестирование, например классический гомогенный тип может быть поводом для выявления антител к двуспиральной ДНК, центромерный тип — для исследования АНА характерных для склеродермии, а гранулярный цитоплазматический тип свечения обычно указывает на наличие антимитохондриальных антител, характерных для первичного билиарного цирроза.
Лабораторные алгоритмы диагностики СЗСТ
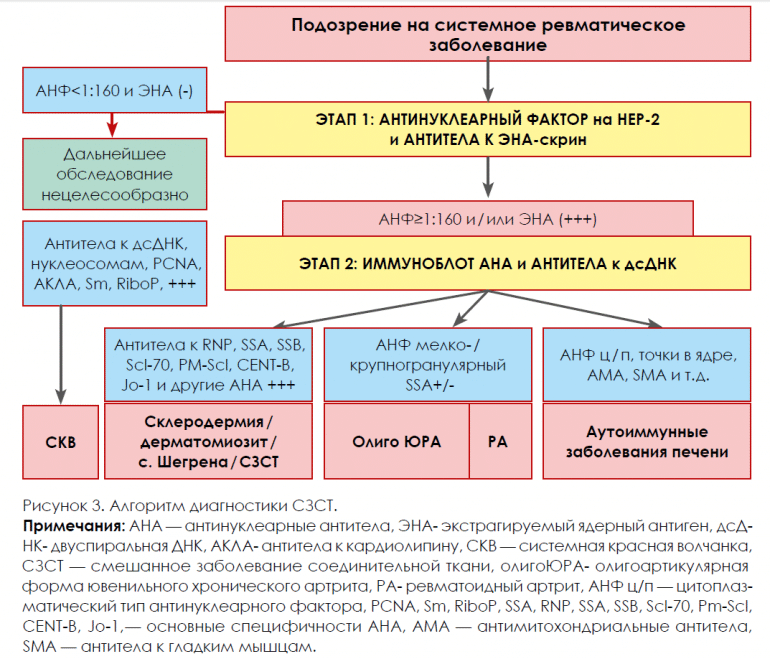
Учитывая разнообразие методов выявление АНА, одновременное назначение всех скрининговых и подтверждающих методов является трудоемким, дорогостоящим и часто неоправданным. Очевидно, что возникает необходимость последовательного тестирования данных АНА, основанном на определенном диагностическом алгоритме. Так как общепринятого алгоритма серологической диагностики АНА у лиц с подозрением на СЗСТ не существует, ряд авторов рекомендуют использовать внутренние алгоритмы, оптимизирующие выявление АНА в рутинной работе. Нами было проведено исследование по разработке и практической оценке алгоритма для диагностики СЗСТ, основанного на результатах обследования 981 пациента в нашей лаборатории. Для выявления АНФ нами был использован метод непрямой иммунофлюоресценции на клеточной линии НЕр-2 и Нер2000 (Euroimmun AG, Германия). Клеточная линия Нер-2000 обладает повышенной частотой клеточных делений, и клетки делятся в 4–10 раз чаще по сравнению с классической линией Нер-2. Для определения АНА с помощью лайнблота использовались диагностические наборы фирмы «Euroimmun AG» (Германия). Данная диагностическая система содержит следующие рекомбинантные антигены: Sm, RNP/Sm, SS-A, SS-B, Scl-70, CENP-B, PCNA, дсДНК, нуклеосомы, гистоны, Jo-1, АМА-М2. Среди исследованных 981 образцов сыворотки крови лиц с подозрением на СЗСТ в 474 образце были выявлены АНА. В данных образцах анализировались результаты выявления АНФ и антител к ЭНА. Хотя оба метода обладают высокой сходимостью, чувствительность определения антител к ЭНА значительно уступает АНФ (20 % против 48 %). Эта находка подчеркивает необходимость использования АНФ для ранней диагностики СЗСТ. Антитела к ЭНА у лиц с подозрением на аутоиммунную патологию были обнаружены в 34 % образцов совместно с АНФ. Изолированно антитела к ЭНА были обнаружены только у 5,5 % (28/507) пациен тов, что указывает на роль тестов для их выявления в определении тех разновидностей АНА, которые утрачиваются из ядра клетки в ходе фиксации, либо плохо распознаются при микроскопии (см. рис. 2). Наряду с определением АНФ и антител к ЭНА мы исследовали данные образцы с помощью лайнблота. Частота положительных результатов лайнблота в зависимости от титров АНФ представлена в таблице 4. В образцах, положительных по антителам к ЭНА, но отрицательных по АНФ антитела к растворимым SS-A/SS-B антигенам отмечались в 64% (18/28) случаев, в образцах положительных по АНФ и анти-ЭНА — в 46 % (136/298) случаев. Кроме того, в двух образцах, изолированно положительных по антителам к ЭНА были обнаружены антитела к Jo-1 антигену, который располагается в цитоплазме клеток и может быть неразличим при микроскопии. Полученные результаты сопоставимы с данными литературы. Специфичность АНА с помощью метода лайнблота была установлена в 63 % образцов, положительных по АНФ и в 97 % образцов, положительных по антителам к ЭНА. Таким образом, специфичность АНА с помощью используемых методов не может быть установлена в 37 % АНФ-положительных образцов, что не исключает диагностической ценности выявления АНФ. Лайнблот оказывается отрицательным у большинства пациентов с низкими титрами АНФ, что совпадает с данными, полученными другими авторами. Таким образом, выполнение лайнблота у пациентов с отрицательным или низким результатом АНФ и отсутствием антител к ЭНА нецелесообразно. Выявление антител к дсДНК обладает высокой сходимостью с результатами определения АНФ и антител к ЭНА. При выявлении АНФ и/или антител к ЭНА вероятность обнаружения антител к дсДНК составляет около 30 %, что позволяет рекомендовать антитела к ДНК в качестве теста «второй линии» при обследовании пациентов с системными заболеваниями, после обнаружения АНФ или антител к ЭНА. Чувствительность ИФА тест-систем по определению антител к дсДНК у различных производителей значительно варьирует, несмотря на то, что для стандартизации данных тестов используется референтная сыворотка Всемирной Организации Здравоохранения (ВОЗ) Wo80. По нашим данным, разница в чувствительности тестов составила 56 % и 38 % в зависимости от производителя. Наряду с методом ИФА в диагностике антител к дсДНК используется метод нРИФ с использованием простейших рода Crithidia lucilliae. Несмотря на сравнительно низкую чувствительность данного метода, этот тест по-прежнему рекомендуется в качестве подтверждающего теста, позволяющего объективизировать выявление антител к дсДНК. Полученные нами данные позволяют рекомендовать сочетанное выявление АНФ методом нРИФ и теста для определения антител к смеси ЭНА в качестве серологического лабораторного скрининга системных заболеваний соединительной ткани. Отрицательный результат обоих методов указывает на отсутствие АНА и делает диагноз СЗСТ маловероятным и не требует дальнейшего применения тестов второй линии, к которым может относиться определение АНА методом лайнблота, метод твердофазного ИФА с раздельными антигенами или методами мультиплексного анализа. При выявлении АНФ или антител к ЭНА рекомендуется использование методов определения специфичности АНА, к которым относится метод лайнблота и определение антител к дсДНК. Проведенный нами финансовый анализ эффективности такого подхода показывает, что использование данного алгоритма сокращает затраты на обследование одного пациента с подозрением на СЗСТ на 33,5 %. Кроме того, последовательное назначение тестов повышает диагностическую эффективность, поскольку снижает число ложноположительных результатов обследования.
Среди СЗСТ по встречаемости АНА системная склеродермия (ССД) даже опережает СКВ, поскольку АНФ отмечается у 95-100 % пациентов с этим заболеванием. К настоящему времени, при ССД описано около 30 антигенных мишеней АНА, причем выявление ряда специфичностей АНА может определять как особенности поражения внутренних органов, так и прогноз заболевания. В большинстве ИФА и блот-тестов обычно присутствует ограниченный спектр антигенов, представленный Scl-70 и CENT-B антигенами, определяющий предрасположенность к диффузной и лимитированой форме заболевания. Фирма Euroimmun AG впервые выпустила набор реагентов, основанный на методе лайн-блота для выявления антител к широкому спектру антигенов, характерных для ССД. С помощью него кроме антигенов Scl-70 и CENT-А и B, входят также антигены РНК-полимераз (RP11 и RP155) которые отмечаются при тяжелом течении ССД, антитела к Th/To, встречающимися при мягкой клинической форме ССД. Также в лайнблоте представлены антигены, характеризующие перекрестные синдромы, в частности Ku, антитела против которого отмечаются при СКВ с симптоматикой ССД и антигены PM-Scl 75кДа и 100 кДа, являющиеся маркером сочетания ССД и полимиозита. Также в состав блота входят ряд антигенов ядрышка (фибрилларин и NOR90), а также антигены PDGFR и Ro-52. Для выявления АНА нами были обследованы 67 больных ССД проходивших стационарное лечение в условиях специализированного ревматологического отделения. В исследованной группе антинуклеарный фактор (АНФ) был выявлен у 100 % (67 /67) пациентов, причем преобладали центромерный и ядрышковый типы свечения ядра. Антитела против Scl-70 и/или анти-CENP-В, которые присутствуют в большинстве тест систем для диагностики системных заболеваний, отмечались в 28 % (19/67) и 34 % (23/67) соответственно, а хотя бы одно из этих антител было обнаружено в 61 % случаев. Использование расширенного лайнблота, содержащего 12 аутоантигенов, позволило определить специфичность АНА в 94 % (63/67), т. е. позволяет увеличить число положительных серологических находок более чем на треть. Таким образом, несмотря на тенденции к автоматизации и попыткам упрощения тестов для серологической диагностики СЗСТ на сегодняшний день наилучшей комбинацией лабораторного тестирования для определения АНА является сочетание выявления АНФ и выявления специфичностей АНА с помощью метода лайнблота с максимально широким спектром аутоантигенов.